PHARMAQ Analytiq har utviklet nye, banebrytende verktøy til bruk i diagnostikk, basert på sekvenseringsteknologien “Next Generation Sequencing” (NGS).

En økende andel av lakseoppdrett benytter seg av lukket- og/eller semilukket produksjon i anlegg som kan ha høy- eller liten grad av resirkulering av vann. Under slike forhold er kontroll på vannkvalitet essensielt for å sikre stabile produksjonsforhold. Selv om fysiske- og kjemiske parameter kan overvåkes nøye, foreligger det lite informasjon vedrørende status på bakteriesammensetningen i vannet, og hvordan denne direkte eller indirekte vil påvirke fiskehelse- og velferd. I tilfeller hvor man har komplekse-, og sammensatte helseutfordringer, hvor årsaken i mange tilfeller er ukjent eller uklar, ser vi at dagens diagnostiske verktøy i mange tilfeller kommer til kort. Med dette som bakteppe, har PHARMAQ Analytiq utviklet nye verktøy til bruk i diagnostikk, basert på sekvenseringsteknologi og en «Next- Generation Sequencing (NGS)» plattform.
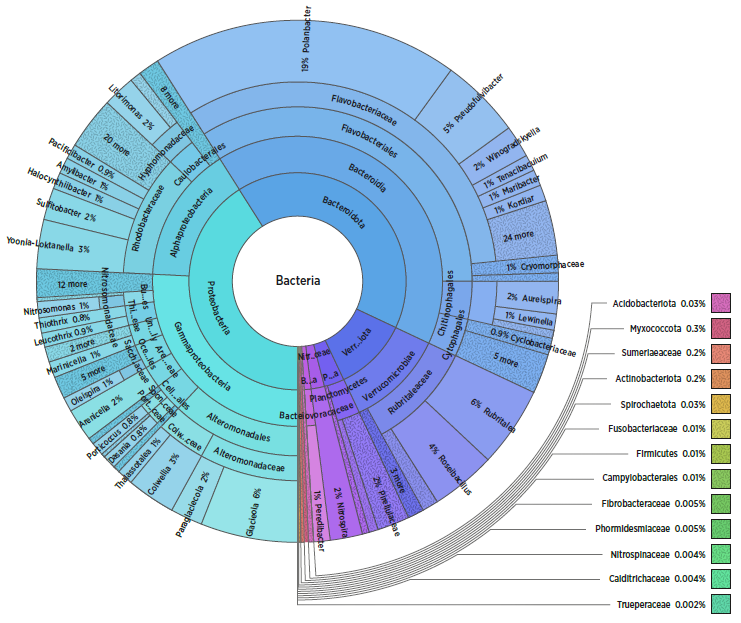
Figur 1. Eksempel på mikrobiell profil fra vannprøve i et produksjonsanlegg. Viser relativt nivå (%) av bakterier på Genus-nivå.

En viktig, og lite kartlagt del av vannkvalitet er mikrobiell sammensetning, og hvordan denne påvirker fiskehelse- og velferd i produksjon. MONMIC prosjektet til SINTEF har vist at kunnskap fra ett anlegg ikke nødvendigvis er direkte overførbart til andre anlegg. Denne variasjonen gjør også at det er utfordrende å definere hva som er normalflora i et anlegg. For å bøte på dette har vi hatt som mål å relatere mikrobiota profiler fra vann- og biofilter til vannkjemi, produksjonsdata og helse data fra et bredt spekter av anlegg- og produksjonsformer. Spesifikke fokusområder innen mikrobiell profilering inkluderer kartlegging av status på inntaksvann (i.e før og etter UV), status på biofilter og status på bakterisammensetning i vann i karene.
Karakterisering av mikrobielle profiler i inntaksvannet gir et godt bilde på hva man kan forvente av bakteriesammensetning i selve karene, men gir også et bilde på eventuell effekt partikkelfjerning og UV-behandling i anlegget har hatt.

Figur 2. Eksempeldata fra inntaksvann. Viser relativt nivå (%) av de ti høyest forekommende bakterier på Genus- nivå for vannprøver tatt ut på ulike dybder.
Biolfilterstatus gir ikke bare en oversikt over alle bakterier tilstede i biofilteret, og relativ mengde av disse, en kan også identifisere andelen nitrifiserende bakterier for å evaluere hvor stabilt filteret er. Et stabilt biofilter, hvor diversiteten av bakterier er høy og ikke endres signfikant av ytre påvirkning.

Figur 3. Eksempeldata fra biofilter profilering. Viser relativt nivå av de ulike nitrifiserende bakteriene på Genus-nivå for prøver tatt fra biofilter.
I vannet hvor fisken oppholder seg vil vi også kunne identifisere bakterielle samfunn, slik som for inntaksvann og biofilter, men også identifisere eventuelle potensielle patogene bakterier som er tilstede, og hvorvidt Geosmin produserende bakterier dominerer.
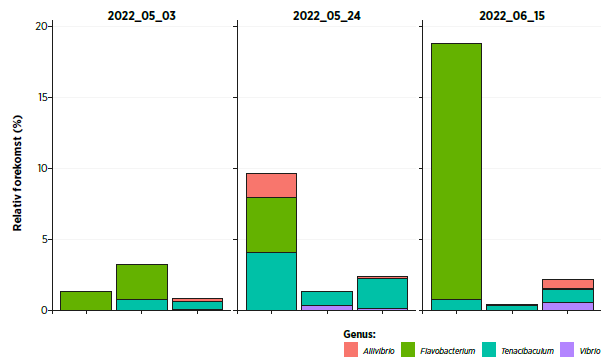
Figur 4. Eksempeldata fra vannprøver i anlegg. Viser relativt nivå (%) av bakterier som inneholder kjente sykdomsgivende arter for laksefisk
Ved å sammenligne resultat fra flere ulike system, med variasjon i temperatur, salinitet, buffer systemer, grad av O2, desinfeksjon osv., vil vi få et bredt og godt grunnlag både for å definere normalflora, og for å identifisere hvilke produksjonparametre som i hovedsak påvirker mikobiota profiler i positiv- eller negativ retning. Selv om vi har ambisjoner om å ha det første vann-flora produktet på plass i 2022, vil det trolig fremdeles være behov for videre datainnsamling i flere år fremover, for bygge kunnskap videre og kontinuerlig forbedre tjenesten.
Problemer med hudsår og gjellesykdom er blant de største tapsårsakene i norsk akvakultur. I begge tilfeller er sykdomsbildet ofte komplekst, med flere patogener tilstede med uavklart årsaksbidrag. Fokus i diagnostikken har i stor grad vært begrenset til dokumentasjon av individuelle patogener tilstede, og hvilken effekt disse har på verten, og liten grad hvordan den totale mikrofloraen på verten bidrar til syksomsbildet. Kartlegging av total mikroflora på hud- og hudssår og gjeller kan bli en nøkkel for å komme videre og få en bedre oversikt over hvilke faktorer som direkte bidrar til sykdom og hvilke som kun opptrer som en konsekvens av sykdom. I prosjektet ønsker vi derfor å kartlegge hud, hudsår- og gjelleflora relatert til ulike produksjons systemer, alder på fisken, vannflora, vannkjemi, temperatur, salinitet mm. Spesielt ved å relatere gjelleflora mot histologisk gjellescore så kan man bygge opp kunnskap om hva som er en god og dårlig gjelleflora. Det vil kreve mye data innsamling og data sammenstilling for å dokumentere korrelasjoner mellom mikroflora- og sykdomsstatus.

Figur 5. Eksempeldata fra svaberprøver tatt fra fisk med- og uten sår. Viser relativt nivå (%) av bakterier tilstede.

Nytten av full genom sekvensering av virus- og bakterier ble veldig tydelig etter inntog av Covid19, der folk flest fikk med seg forskjellen mellom delta-variant og omikron-varianten av viruset og at disse endringene kunne påvirke effekten av vaksineprogrammene. Man har samme problemstilling på fisk, der virus og bakterier stadig er i endring.
De fleste fisk er vaksinert mot 5-7 agens. Vaksineselskapene har en kontinuerlig jobb med å overvåke om deres vaksine dekker de til enhver tid sirkulerende typene av virus og bakterier. NGS basert karakterisering vil gi en mye mere detaljert kunnskap om hvilke bakterier og virus som til enhver tid påvises i norsk fiskeoppdrett, og dette vil gi en mye bedre oversikt og mulighet til bekjempelse.

Figur 6. Eksempeldata på helgenom sekvens fra bakterie isolert fra felt.
Kombinerer vi denne informasjonen med geografisk utbredele og produksjonsform, kan informasjonen også benyttes for utvikling av verktøy for molekylær sporing av smitteveier og identifisering av opphav for smitte (Molekylær sporing). Slik kunnskap er selvsagt helt avgjørende når man skal treffe tiltak for bekjempelse og forebygging.
Kunder oppfordres til å ta kontakt i planleggingsfasen av prosjekter. Vårt team kan bidra med rådgivning rundt prøvetaking, design og valg av analyser for å optimalisere forsøksoppsettet i henhold til målsetting for prosjektet.
Kundeprosjekter
PHARMAQ er verdens ledende selskap innen vaksiner og innovasjon rettet mot akvakulturnæringen og er en del av Zoetis, verdens ledende selskap innen dyrehelse. Våre innovative fiskehelseløsninger inkluderer et bredt spekter som fiskevaksiner, terapiprodukter, vaksinasjonsmaskiner inkludert servicetjenester, forskning og analyser. Selskapet leverer miljøvennlige, trygge og effektive helseprodukter til den globale akvakulturnæringen ved hjelp av målrettet forskning og engasjerte medarbeidere. Produksjon, administrasjon, forskning og utvikling ligger i Norge og med global virksomhet i kommersielle oppdrettsmarkeder har PHARMAQ rundt 375 medarbeidere. Konsernets produkter markedsføres i Europa, Nord- og Sør-Amerika samt i Asia. For mer informasjon, se selskapets hjemmeside: www.pharmaq.com. Personvernerklæring Erklæring om informasjonskapsler (cookies) Bruksvilkår
Copyright © 2020 Zoetis LLC. Alle rettigheter forbeholdt.